- 首页 > 单细胞重测序
单细胞重测序
单细胞研究概述
目前测序技术已经深入到人类疾病健康、物种进化、动植物分子育种等传统的生物学研究领域中,逐渐成为一种不可或缺的研究工具。然而随着生命科学和医学基础研究的深入发展,人们发现越来越多的特殊标本和特定的生物学现象,如法医鉴定的微量标本、肿瘤内部异质性等无法用常规组织测序的方法进行研究。为了更好的处理这些标本和研究这类现象背后的机理,科学家经过不懈的努力,从而产生了单细胞扩增和分析技术。单细胞技术在人类疾病健康研究的应用将更好地揭示它们的发生发展过程和规律, 从而有助于人类疾病的认识、预防、诊断和治疗。
研究流程

图1 单细胞DNA技术研究流程图
单细胞DNA扩增技术比较
|
MALBAC |
MDA |
|
|
扩增的DNA长度 |
0.5-1.5kbp |
2-100kbp |
|
人工序列引入 (Induced
artificial sequence) |
70bp = 35bpx2 (作为引物 => ~7% 数据浪费) |
不存在 |
|
覆盖度 (>25X时) |
84%~93% |
>95% |
|
假阳性率 |
4X10^-5 |
1X10^ |
对于MDA和MALBAC两种技术,我们检测了低深度下的数据质量。如下是我们测试的结果:
|
单细胞1* (MDA) |
单细胞2* (MALBAC) |
|
|
比对率(%) |
92.81 |
88.45 |
|
全基因组覆盖度(%) |
7.935 |
7.09 |
*样品选择:第一例亚洲人基因组供体(炎黄)的类淋巴母细胞细胞系的单细胞;
*数据设置:分别用MDA和MALBAC技术对两个重复做0.1X深度的扩增;
从结果可以看出,低深度数据下,MDA的Mapping率和覆盖度都优于MALBAC方法法。我们的MDA方法的数据有效性也略优于MALBAC(reads会截取35bp的数据浪费)方法。高深度的测序(MDA技术)非常适合SNV检测。
文库及测序策略
文库构建策略: 根据研究目的构建人重、外显子、目标区域文库
测序策略:DNBSEQ平台 PE150
推荐数据量:
针对大批量细胞的测序,可以进行低深度潜覆盖测序;对于细胞之间亲缘关系较大的,可以适量增加测序深度。
针对小规模细胞测序,研究功能性变化的,可参考常规全基因组重测序/外显子组测序/目标区域测序的测序深度。
其余个性化研究目的,测序深度视不同的研究目的可适度调整。
信息分析内容(建议30X以上覆盖深度)
- 去除接头污染序列及低质量数据
- 比对,产出数据统计
- SNP检测、注释和统计
- InDel检测、注释和统计
- SV检测、注释和统计(仅全基因组测序)
单细胞测序发现一例结肠癌为双克隆起源,不同克隆展现不同的突变特征
Discovery of biclonal origin and a novel oncogene SLC12A5 in colon cancer by single-cell sequencing
案例描述:
深圳华大基因研究院联合香港中文大学合作、北京大学肿瘤医院/研究所的研究人员,对一例T3N0M0结肠癌病人的63个肿瘤单细胞、4个正常单细胞样本进行外显子测序。单细胞群体遗传学分析发现肿瘤细胞群体存在两个克隆群体,不同克隆具有不同的突变特征。
部分研究成果:
群体遗传学分析发现该例肿瘤为双克隆起源。其主要克隆群体发生了APC、TP53突变,次要克隆群体CDC27和PABPC1为主要突变,但APC和TP53未发生突变。
单细胞水平发现SLC12A5为高频突变,但群体水平突变率极低。功能验证发现SLC12A5可能对结肠癌具有致癌效应。
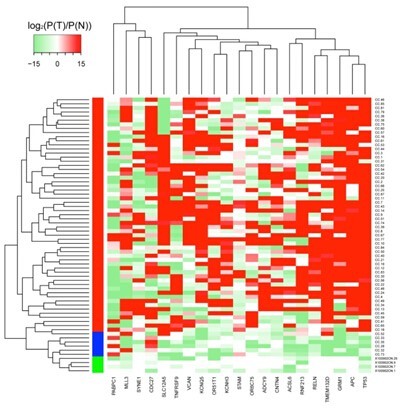
图1 结肠癌单细胞不同克隆群体的driver event分析
对结肠癌单细胞及另外21例结肠癌的变异结果进行分层聚类,发现major clone (red)主要包含TP53和APC,而minor clone (blue)主要包含CDC27和PABPC1,normal cells (green)不含突变。
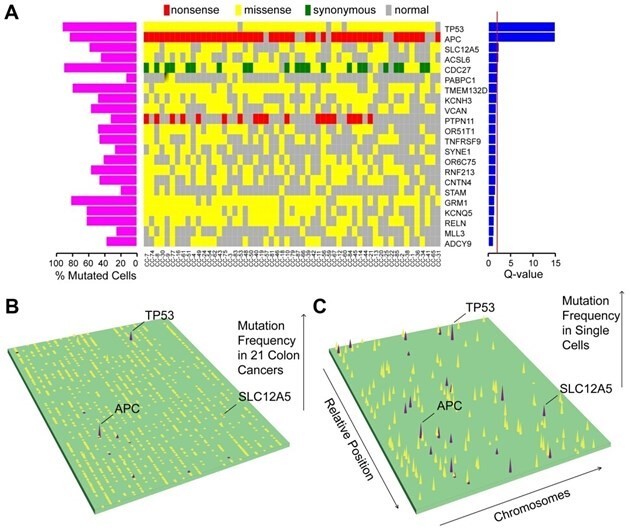
图2 突变图谱及dirver genes预测
(A) major clone中体细胞突变。左侧代表突变频率,右侧表示预测的driver genes Q-score; (B) 21例结肠癌的体细胞突变图谱,尖峰高度代表突变频率; (C) 结肠癌单细胞的突变图谱。
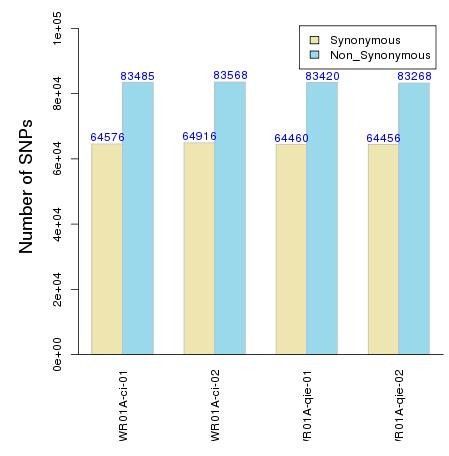
图1 同义和非同义snp统计图
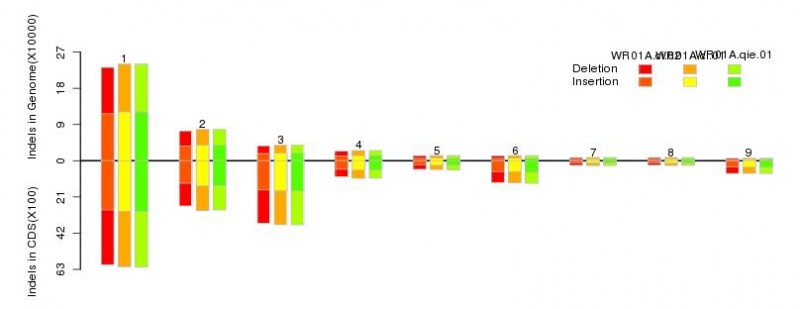
图2 基因组和编码区域InDels分布图
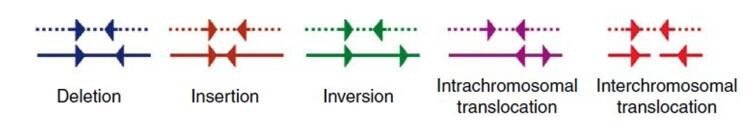
图3 存在结构变异的read对
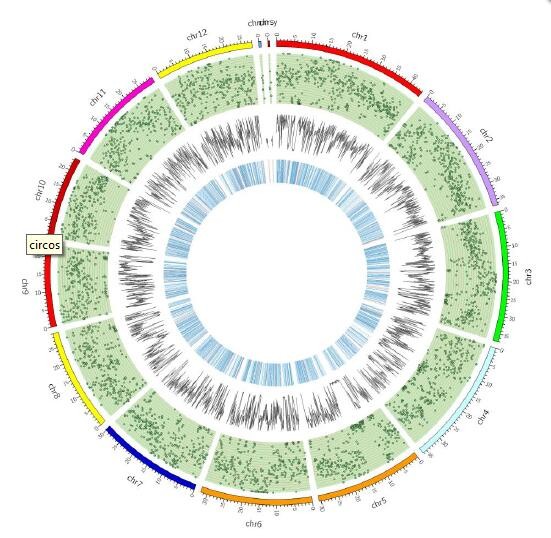
图4 变异在基因组上分布统计
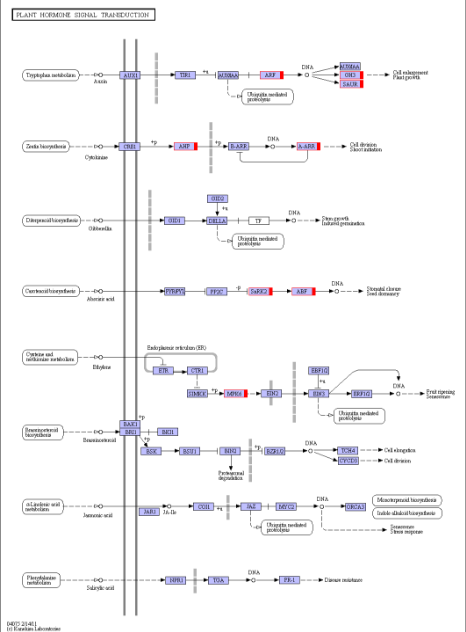
图5 变异基因通路代谢图
样品要求
主要针对人和小鼠样品。若为其他物种,需要客户提供看家基因检测引物。
样品准备
1) 将细胞分选至装有3~5μL PBS缓冲液的200μL PCR管中,细胞数目不得超过1000个。不建议另外加入其他细胞保护剂,如有特殊情况,加入其他试剂或者经过其他处理,请在样品信息单中备注。
2) 细胞分离完成后,请于10分钟内放入-80℃冰箱或者干冰保存。也可暂存于-20℃,但保存时间不得超过3小时。
3) 每个细胞样品建议送4管重复,以保证后续实验成功率。例如:需测序某一细胞样品数为5个,则建议送样细胞样品管数为20。
4) 除提供细胞样品外,还需要每批次提供一个阴性对照,即在PBS缓冲液中加入0.1~0.5 μL的1% PBS-BSA溶液(分选细胞时,细胞所处保存溶液)。
表1 单细胞DNA测序送样要求
|
测序类型 样品类型 |
WGS |
WES/目标区域测序 |
|
单细胞 |
1-2个(4μL
PBS悬液) |
1-2个(4μL
PBS悬液) |
|
微量细胞 |
2≤X≤1000(4μL
PBS悬液) |
2≤X≤1000(4μL
PBS悬液) |
注:X为细胞数目
Q1:单细胞重测序大致流程如何?
单细胞分离(口吸管法)→单细胞裂解提取DNA→单细胞全基因组扩增→建库测序→信息分析。
Q2:单细胞分离方法有哪些?
单细胞分离主要有四种方法:激光显微切割、流式细胞仪分选、微流控芯片分选和口吸管法分离。流式细胞仪需要对细胞进行染色和处理,可能影响全基因组扩增效果。目前华大采用的是口吸管法分离,该方法很大限度地避免了细胞损坏,还原细胞较真实的状态。华大在单细胞分离扩增经验非常丰富,现在已经完成了上万个细胞的分离与扩增。
Q3:单细胞是由客户还是华大分离?
推荐客户送分离好的单细胞,并溶解在华大提供的裂解液当中。
Q4:单细胞肿瘤研究如何避免癌细胞取样的假阳性?
华大对单细胞不经过任何染色,在显微镜下无法识别细胞是肿瘤细胞还是正常细胞,建议客户取样前通过病理学的方法估计肿瘤组织的纯度,我们一般要求纯度高于80%。虽然后期信息分析能排除肿瘤组织中正常细胞的干扰,但是肿瘤细胞含量较低需要选取的细胞总量将会增多,这会加大项目投入。
Q5:经过全基因组扩增之后可以得到多少基因组 DNA ?
全基因组扩增后可以得到3-5μg的DNA量,达到一般建库测序的DNA量要求,可用于各种常规的重测序。
Q6:单细胞扩增实验的成功率如何?
受样品质量或细胞状态的影响,可能造成全基因组扩增实验失败。根据实验的经验,现在我们的扩增成功率大概在50%,因此每例样品实际扩增的细胞数量需为测序细胞数量的2倍以上,例如项目设计方案确定对该样品的50个单细胞进行测序和分析,则至少需提供100个细胞。
Q7:华大对扩增产物质控指标如何?
全基因组扩增中扩增不均会导致测序覆盖度低,为确保数据利用率,全基因组扩增实验后须对扩增产物进行质控。我们通过PCR方法对管家基因进行检测。检测结果必须保证8个管家基因有6个以上阳性,反之则属不合格样品不能用于建库测序。现阶段管家基因质控的指标仅限于人,其他物种的还需要开发。此外我们还参考一般的DNA重测序送样要求对扩增产物进行质控。
Q8:华大采用的全基因组扩增技术如何?
单细胞扩增主要有两种类型的技术:基于热循环以PCR为基础的扩增技术,如简并寡核苷酸引物PCR (Degenerate oligonucleotide primer PCR, DOP-PCR)、连接反应介导的PCR (ligation mediated PCR, LM-PCR)、扩增前引物延伸反应 (Primer extension preamplification, PEP)等;基于等温反应不以PCR为基础的扩增技术,如多重置换扩增 (Multiple displacement amplification, MDA)、基于引物酶的扩增 (Primase-based whole genome amplification, pWGA)。前者以DOP-PCR为代表,具有扩增均一性较高的优点,不足之处是扩增覆盖度较低。后者以MDA为代表,该技术基于phi29酶在恒温条件下进行扩增。该酶对于模板有很强的结合能力,能连续扩增10Kb 的DNA片段而不从模板上解离,同时这种酶具有3’→5’外切酶活性,错误率仅为5 x 10-6,大约比Taq DNA聚合酶低100倍,因此可以保证扩增的高保真性。华大单细胞全基因组扩增基于MDA技术,具有扩增产物长(大于10kb),覆盖度高(一般不低于70%,可达90%以上),扩增错误率低(仅为10-6),具有高特异性和灵敏性的特点。
Q9:MDA扩增的特点如何?
MDA具有扩增产物长、覆盖度高、扩增错误率低的优点,此外还存在两个主要的不足:扩增均匀性和等位基因丢失。基因组上GC含量越高扩增效率越高,导致高GC含量的区域测序深度远高于其他地方,呈现出明显的扩增偏向性。除了存在扩增偏向性之外,在扩增过程中还存在等位基因丢失的问题(Allele dropout ,ADO,单细胞基因组上杂合的等位基因在扩增过程中会只扩增出其中一个等位基因,导致另外一个等位基因丢失的现象)。针对这些问题华大升级了扩增的方法,使得基因组上均一性比之前有了很大的提高;并且ADO也从之前Cell文章外显子数据的平均43%降低到5%以下(小试数据),大大降低了偏向性和ADO对下游信息分析的影响。(详细信息请看新方法测评结果)。
Q10:单细胞DNA测序可以做哪些变异检测?
单细胞经过全基因组扩增之后合格的扩增产物可以进行全基因组测序、外显子测序、目标区域捕获测序。不同的测序类型可以进行不同类型的变异检测,外显子测序和目标区域捕获测序只能进行SNP和Indel的检测;全基因组测序则能进行所有类型的变异检测,如SNP、Indel、CNV、SV,全面地反馈单细胞水平上的所有变异类型。

